Ảnh Hưởng Của COVID-19 Lên Diễn Tiến Bệnh Gan
Tổng quát
Hội chứng hô hấp cấp tính nghiêm trọng do coronavirus-2 (SARS-CoV-2) là một loại coronavirus mới gây ra bệnh do coronavirus 19 (COVID-19), đã lây nhiễm cho hàng triệu người trên toàn thế giới chỉ trong vài tháng. Một số ít, nhưng đáng kể, những người bị nhiễm bệnh cần phải nhập viện và chăm sóc đặc biệt. Ngay từ khi bắt đầu xảy ra đại dịch vi rút mới này, rõ ràng những người béo phì và / hoặc tiểu đường có tiên lượng xấu về sự tiến triển của COVID-19, cho thấy rõ ràng mối liên quan giữa bệnh gan và COVID-19 nghiêm trọng. Bởi vì bệnh gan mãn tính (CLD) có liên quan đến rối loạn điều hòa miễn dịch và viêm, không có gì ngạc nhiên khi bệnh nhân CLD có thể có nguy cơ bị các kết cục bất lợi cao hơn sau khi nhiễm SARS-CoV-2. Dữ liệu COVID-19 ban đầu cũng chỉ ra rằng những người khỏe mạnh bị nhiễm có các xét nghiệm chức năng gan bất thường, cho thấy có thể có tác động trực tiếp của SARS- CoV-2 đến tổn thương gan. Ở đây chúng tôi cho thấy COVID-19 ảnh hưởng đến sự chuyển hóa của gan và làm tăng tỷ lệ mắc bệnh và tử vong ở những người mắc bệnh CLD nền. (Hepatology Communications 2021; 0: 1-13)
Hội chứng hô hấp cấp tính nghiêm trọng trong đại dịch coronavirus 2 (SARS-CoV-2) nhấn mạnh tầm quan trọng của một phản ứng miễn dịch hiệu quả trên vật chủ. (1) SARS-CoV-2 gây ra bệnh coronavirus 2019 (COVID-19), có thể liên quan đến một số các triệu chứng đa dạng, bao gồm rối loạn điều hòa miễn dịch và cơn bão cytokine. Trong COVID-19, nồng độ cytokine tăng cao có liên quan đến tổn thương phổi và suy đa cơ quan, (2) và cơn bão cytokine nghiêm trọng hơn có thể góp phần gây bệnh sinh COVID-19. (3,4) Cytokine tăng cao ở bệnh nhân COVID-19 bao gồm interleukin (IL) -1β, interleukin-6, interferon (IFN) – γ sản xuất protein 10, yếu tố hoại tử khối u (TNF), IFN-γ, protein viêm đại thực bào 1α và 1β, và yếu tố tăng trưởng nội mô
mạch máu.(5) Đặc biệt, mức IL-6 cao có liên quan đến mức độ nghiêm trọng và tử vong của COVID-19.(6) Mặc dù bệnh nhân mắc COVID-19 có các phản ứng miễn dịch rất thay đổi và các triệu chứng liên quan đến miễn dịch, những người không thể kiểm soát sự sao chép của SARS-CoV-2 có nhiều khả năng bị rối loạn điều hòa miễn dịch liên quan đến bệnh sinh (Hình 1).
Ngoài ra còn có đại dịch béo phì trên toàn thế giới đang diễn ra dẫn đến tình trạng kháng insulin, tiểu đường và bệnh gan mãn tính (CLD), trở thành gánh nặng sức khỏe cộng đồng lớn. (7,8) CLD thường gặp nhất do viêm gan B và C mãn tính, bệnh gan liên quan rượu (ALD) và bệnh gan nhiễm mỡ không do rượu (NAFLD). CLD có thể tiến triển thành viêm (viêm gan nhiễm mỡ không do rượu [NASH]), xơ hóa, và cuối cùng là xơ gan và ung thư biểu mô tế bào gan (HCC) như những bệnh ở giai đoạn cuối. Xơ gan, viêm gan siêu vi và HCC gây ra khoảng 2 triệu ca tử vong mỗi năm trên toàn thế giới. (7,8) Tế bào gan, chủ yếu là tế bào gan, tạo thành một nguồn protein chính liên quan đến các phản ứng miễn dịch bẩm sinh và đáp ứng.
Gan điều chỉnh cân bằng nội môi miễn dịch bằng cách ngăn chặn sự lây lan có hệ thống của các kháng nguyên vi sinh vật và chế độ ăn uống đến từ ruột, và thông qua việc tổng hợp các phân tử hòa tan cần thiết cho các phản ứng miễn dịch hiệu quả. (9) Do đó, tổn thương gan có thể dẫn đến khả năng giám sát miễn dịch bị tổn hại do giảm sự tổng hợp tại gan, các protein liên quan đến miễn dịch bẩm sinh và nhận dạng mô hình phân tử liên quan đến mầm bệnh.
Cả CLD và xơ gan đều được đặc trưng bởi rối loạn điều hòa miễn dịch. (10) CLD gây suy giảm vai trò cân bằng nội môi của gan trong phản ứng miễn dịch toàn thân. Các mô hình phân tử từ các tế bào gan bị tổn thương thúc đẩy các tế bào miễn dịch tuần hoàn gây ra viêm hệ thống, dưới dạng các tế bào miễn dịch tuần hoàn được kích hoạt và tăng nồng độ trong huyết thanh của các cytokine tiền viêm (ví dụ, TNF và IL-6). Quan trọng là, rối loạn chức năng miễn dịch liên quan đến gan có thể làm tăng tính nhạy cảm với các bệnh nhiễm trùng. Trong bối cảnh này, không có gì ngạc nhiên khi bệnh nhân CLD, đặc biệt là những người bị xơ gan mất bù, có nguy cơ mắc bệnh và tử vong liên quan đến COVID-19 cao hơn.(11) Sự kết hợp giữa nhiễm trùng
SARS-CoV-2 và xơ gan dường như là một bộ đôi gây chết người, có thể là do sự kết hợp của các quá trình sinh học được đặc trưng bởi rối loạn điều hòa miễn dịch (Hình 2). Điều quan trọng là, ghép gan phục hồi chức năng gan ở bệnh nhân xơ gan mất bù, do đó làm giảm nguy cơ tử vong do COVID-19 đối với dân số nói chung. (12)
Ngoài tác động tiên lượng xấu của CLD ở bệnh nhân COVID-19, nhiễm trùng SARS-CoV-2 cũng có thể ảnh hưởng tiêu cực đến sức khỏe gan ở những người khỏe mạnh trước đó. Dữ liệu lâm sàng hiện có chỉ ra rằng những bệnh nhân có COVID-19 thường có các xét nghiệm chức năng gan bất thường, chẳng hạn như aspartate transferase (AST) và alanin transferase (ALT). (13) Tuy nhiên, cơ chế tác động của COVID-19 lên chức năng gan là chưa được hiểu đầy đủ và có thể là đa yếu tố, và người ta chưa chứng minh được rõ ràng liệu SARS-CoV-2 có thể lây nhiễm tế bào gan hay không. Bởi vì tổn thương gan cấp tính hoặc ứ mật có thể phát triển trong các trường hợp nghiêm trọng của cơn bão cytokine, (1,14) không liên quan đến COVID-19, có thể rối loạn điều hòa miễn dịch có nguồn gốc SARS-CoV-2 có thể đóng một vai trò trong bệnh lý gan liên quan đến COVID-19 .
Mục đích của chúng tôi là ở đây để xem xét và thảo luận về tác động của COVID-19 đối với những người có gan khỏe mạnh cũng như những rủi ro của COVID-19 nghiêm trọng ở những bệnh nhân bị bệnh gan nhiễm mỡ, viêm gan virus, xơ gan, HCC, ALD và những người ghép gan. Hiệu quả của các liệu pháp kháng vi-rút và chống viêm COVID-19 đối với gan cũng sẽ được xem xét và xem xét kỹ lưỡng.
Tác động của COVID-19 ở những người có gan khỏe mạnh
Như đã đề cập trước đây, bệnh nhân có COVID-19 thường biểu hiện tăng cao các dấu hiệu liên quan đến tổn thương gan, chẳng hạn như AST, ALT, phosphatase kiềm và gamma-glutamyltransferase (GGT).(13,15-17)
Giá trị tiên lượng của các dấu hiệu tổn thương gan tăng cao ở bệnh nhân COVID-19 vẫn còn gây tranh cãi, như được xem xét bởi Bertolini và cộng sự, (13) với một số nghiên cứu cho thấy rằng giá trị AST hoặc ALT tăng cao có tương quan với tình trạng tiên lượng xấu, trong khi những người khác không tìm thấy mối liên quan với sự tiến triển hoặc tử vong của COVID-19.
Một cơ chế có thể gây ra tổn thương gan được quan sát thấy ở bệnh nhân COVID-19 là nhiễm trùng gan trực tiếp bởi SARS-CoV-2. Thụ thể tế bào chủ SARS CoV-2 là men chuyển 2 (ACE2), (18) và sự xâm nhập tế bào SARS-CoV-2 cũng liên quan đến protease serine xuyên màng 2. (TMPRSS2). (18)

HÌNH 1. Đặc điểm sinh lý bệnh của nhiễm trùng SARS-CoV-2. Sau khi nhiễm SARS-CoV-2, cơn bão cytokine có thể xảy ra do nhận dạng mầm bệnh không thích hợp hoặc không hiệu quả, với sự lẩn tránh miễn dịch tạo ra phản ứng không thích hợp, bao gồm phản ứng tác động phóng đại, sản xuất cytokine và / hoặc không trở lại cân bằng nội môi. Các con đường được mô tả dựa trên một báo cáo của Fajgenbaum và June. (1) Ví dụ về các loại thuốc có thể ức chế các con đường truyền tín hiệu được hiển thị bằng màu đỏ. Các từ viết tắt: JAK-STAT3: Janus kinase-đầu dò tín hiệu và chất kích hoạt phiên mã 3; MAPK, proteinkinase hoạt hóa mitogen; mTOR, mục tiêu của rapamycin trên động vật có vú; NF-κB, yếu tố hạt nhân kappa B; Treg, tế bào T điều hòa.
Các nghiên cứu giải trình tự cho thấy biểu hiện ARN messenger ACE2 (mRNA) trong một quần thể phụ của tế bào mật, nhưng không có hoặc biểu hiện tối thiểu trong tế bào gan và không biểu hiện ở các loại tế bào gan khác. (19-22) Biểu hiện mRNA TMPRSS2 đã được tìm thấy trong một nhóm nhỏ các tế bào gan và tế bào mật. (23,24) Protein ACE2 không được phát hiện trong tế bào gan. (25) Những phát hiện này cho thấy rằng SARS-CoV-2 không trực tiếp gây ra tổn thương tế bào gan. Điều thú vị là SARS-CoV-2 có thể tái tạo trong dòng tế bào HCC Huh-7. (26) Ngoài ra, các hạt SARS CoV-2 không có túi bọc màng đã được phát hiện trong tế bào chất của tế bào gan từ 2 bệnh nhân có COVID-19 có các dấu ấn tổn thương gan tăng cao(27)
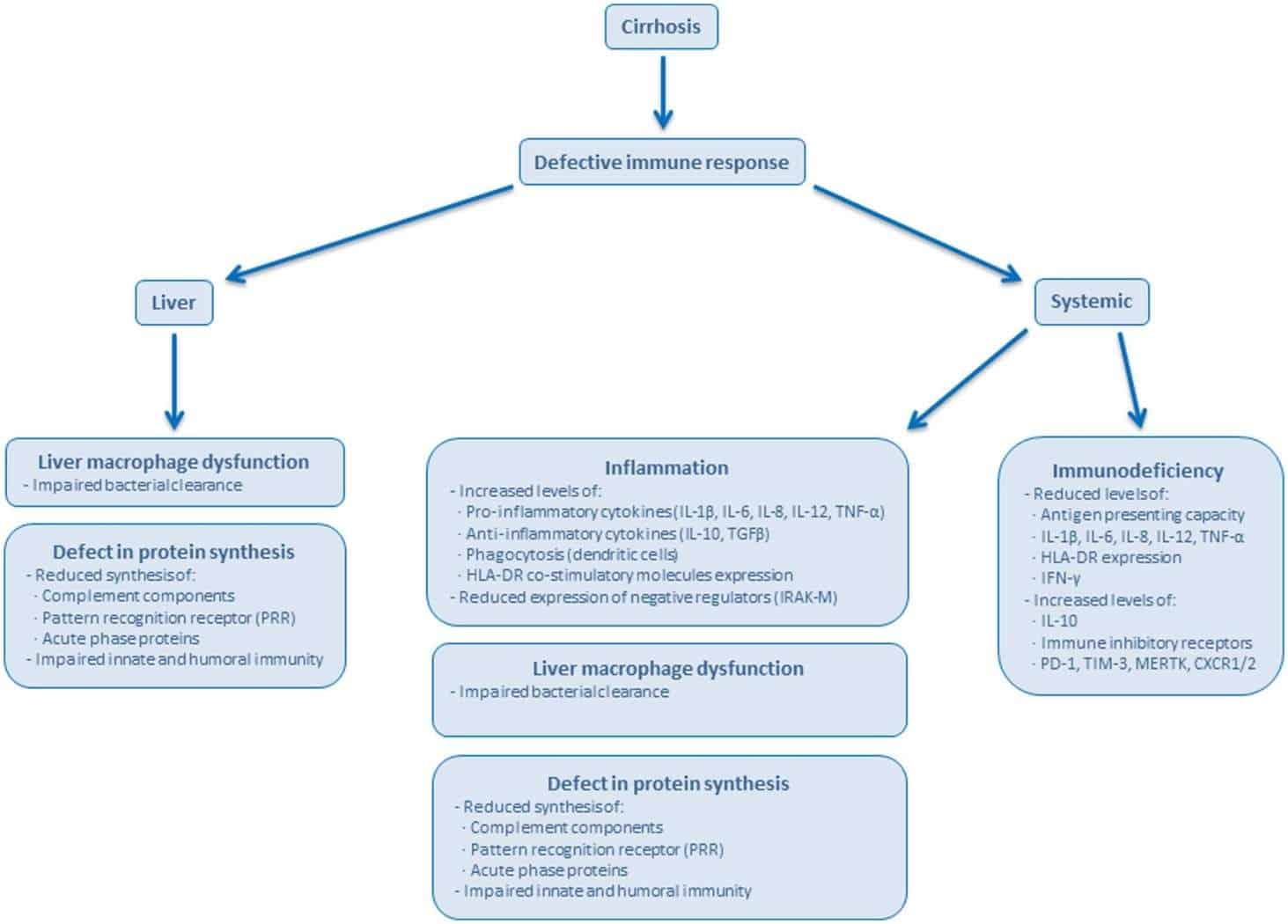
Hình. 2. Đặc điểm suy giảm miễn dịch thường thấy ở bệnh nhân xơ gan. Xơ gan phá vỡ cấu trúc gan và tổ chức tế bào, giảm khả năng tổng hợp protein của gan. Xơ gan ảnh hưởng đến chức năng tuần hoàn và đường ruột của các tế bào miễn dịch, dẫn đến một số bất thường ảnh hưởng đến các thành phần tế bào và các chất hòa tan của phản ứng miễn dịch cả ở gan và hệ thống. (10) Viết tắt: CXCR1 / 2, thụ thể chemokine 1/2 ; HLA-DR, kháng nguyên bạch cầu người-DR; IRAK-M, kinase 3 liên kết với thụ thể interleukin; MERTK, c-mer proto-oncogene tyrosine kinase; PD-1, tế bào chết được lập trình-1; TGF-β, yếu tố tăng trưởng biến đổi β; TIM-3, globulin miễn dịch tế bào T và miền mucin- 3.
Tuy nhiên, các mẫu này không được đánh giá về sự hiện diện của RNA virus để loại trừ nguồn gốc khác của các phần tử này. (28) Đáng chú ý, SARSCoV-2 có thể lây nhiễm mô liên quan đến ruột, (29,30) và một số bệnh nhân bị COVID-19 (< 15%) biểu hiện RNA virus trong máu của họ.(31,32) Do đó, người ta cho rằng vi rút có thể xâm nhập vào hệ thống tuần hoàn cửa, do đó đến gan, và các tế bào Kupffer có thể cố gắng loại bỏ vi rút và tạo ra viêm cục bộ. (13)
Gan cũng có thể bị ảnh hưởng bởi tình trạng thiếu oxy và cơn bão cytokine sau nhiễm trùng SARS-CoV-2, có liên quan đến suy đa cơ quan ở một số bệnh nhân bị COVID-19.(1,33) Cơn bão cytokine cũng có thể liên quan đến đông máu nội mạch lan tỏa (DIC) và giảm tiểu cầu, có thể làm trầm trọng thêm các biến chứng DIC, như được quan sát thấy trong COVID-19. (34) Những bệnh nhân COVID-19 có biểu hiện viêm nội mô trong gan, (35) fibrin microthrombi trong xoang gan, (36,37) và hoạt hóa hệ thống bổ thể. (38) Một báo cáo đã chứng minh rằng, trái ngược với những bệnh nhân bị COVID-19 nhẹ, những bệnh nhân bị viêm phổi không phải COVID-19 không cho thấy mức độ tăng của AST, ALT hoặc GGT, (39) cho thấy rằng bệnh nhân bị COVID- 19 nhẹ có thể có các dấu hiệu tổn thương gan tăng cao độc lập với sự hiện diện của viêm.
Mô hình sinh hóa gan bất thường lúc nhập viện và trong quá trình bệnh ở bệnh nhân nhập viện nhiễm COVID-19 được phân tích có liên quan đến tăng men aminotransferase chiếm ưu thế AST. (40) Phát hiện này gợi ý một cơ chế tổn thương gan qua trung gian đặc hiệu với virus. Kết quả này trái ngược với kết quả quan sát được ở bệnh viêm gan do vi rút, vốn thường dẫn đến tổn thương gan do ALT chiếm ưu thế. AST được tạo ra trong cơ và những bệnh nhân bị COVID-19 có dấu hiệu của chấn thương cơ. Sự gia tăng chủ yếu AST cũng liên quan đến ALD, thiếu máu cục bộ và xơ gan, cho thấy tác động của COVID-19 đối với gan. Tăng AST và GGT cũng có liên quan đến nhiễm vi-rút cúm và tổn thương qua tế bào liên quan. (41) Hóa sinh gan có liên quan đến mức độ nghiêm trọng và kết quả lâm sàng của COVID-19.
Tuy nhiên, tác động của COVID-19 đối với một lá gan khỏe mạnh dường như không đáng kể và chỉ giới hạn ở những bệnh nhân bị nhiễm trùng nặng và suy đa cơ quan.
(42,43)
Độc tính trên gan của Liệu pháp chống viêm và kháng vi-rút COVID-19
Một nguồn khác có thể gây tổn thương gan ở bệnh nhân COVID-19 là tổn thương gan do thuốc liên quan đến các liệu pháp COVID-19. Một nghiên cứu báo cáo rằng trong số những bệnh nhân có COVID-19 có dấu hiệu tổn thương gan bình thường khi nhập viện, gần một nửa đã phát triển nồng độ dấu hiệu gan bất thường sau 1 tuần sau khi nhập viện. (44) Điều trị bằng Lopinavir-ritonavir có liên quan đến mức tăng AST, ALT, và bilirubin (45); remdesevir được báo cáo là gây tăng cao AST và ALT (46,47); và acetaminophen và hydroxychloroquine có liên quan đến các dấu hiệu gan bất thường. (48,49) Độc tính với gan của remdesivir đã được tranh luận rộng rãi. Các thử nghiệm ngẫu nhiên đã chỉ ra rằng sự gia tăng men gan tương đương giữa các nhóm được điều trị bằng remdesivir và nhóm chứng. (47) Tuy nhiên, cơ sở dữ liệu báo cáo an toàn của WHO chỉ ra một tỷ lệ chênh lệch có ý nghĩa thống kê đối với tổn thương gan khi sử dụng remdesivir.(50) Các chất ức chế men chuyển cũng đã được khám phá là phương pháp điều trị COVID-19 có thể. Những thuốc cũng làm tăng nồng độ men gan. (45) Thật không may, các loại thuốc cũ được sử dụng lại dường như không có tác động đến COVID-19. (51) Mặt khác, các chất điều hòa miễn dịch dường như là một chiến lược điều trị hiệu quả hơn để điều trị bệnh tật và tử vong do COVID-19 — với corticosteroid, chẳng hạn như dexamethasone, làm tăng đáng kể tỷ lệ sống sót và giảm tỷ lệ mắc bệnh ở những bệnh nhân nhập viện với COVID-19 (52) và ở những bệnh nhân bị COVID-19 vừa hoặc nặng. (53) Vì corticosteroid có nguồn gốc từ quá trình chuyển hóa cholesterol, có thể can thiệp vào nhiều khía cạnh của cân bằng nội môi glucose, nên cần chú ý đến những ảnh hưởng có thể có của các hợp chất này đối với chuyển hóa gan và nhiễm mỡ gan. (52) Thật vậy, điều trị bằng corticosteroid trong COVID-19 nặng có liên quan đến tổn thương gan đáng kể. (54) Tocilizumab, một kháng thể đơn dòng được nhân tính hóa chống lại thụ thể IL-6, được sử dụng để điều trị viêm khớp dạng thấp và hiện được sử dụng nhiều để chống lại tổn thương qua trung gian cytokine trong COVID-19 nghiêm trọng, cũng được biết là gây tăng ALT đáng kể. (55) Nghiên cứu hồi cứu này báo cáo rằng nhóm tocilizumab có mức tăng ALT cao hơn đáng kể. (55) Cuối cùng, thuốc kháng sinh, là một trong những nguyên nhân phổ biến nhất của tổn thương gan do thuốc, cũng có thể góp phần gây tổn thương gan ở bệnh nhân COVID-19.
Gần đây, một nghiên cứu hồi cứu khác bao gồm 1.040 bệnh nhân mắc COVID-19 đã phát hiện thấy mức ALT / AST tăng cao ở 22,6% số người tham gia nghiên cứu. (56) Trong nhóm này, việc sử dụng lopinavir – ritonavir, có hoặc không có ribavirin, IFN- β và / hoặc corticosteroid, có liên quan độc lập với tăng ALT / AST. Thuốc kháng vi- rút SARS-CoV-2 đặc hiệu mới hiện đang trong giai đoạn thử nghiệm lâm sàng 3 (ví dụ: molnupiravir), (57) và chúng có thể sớm đưa vào phòng khám. Các nghiên cứu trong tương lai sẽ có giá trị tiến hành xác định những ảnh hưởng có thể có của các loại thuốc SARS-CoV-2 mới đối với chức năng gan ở bệnh nhân COVID-19. Cụ thể, các cá nhân bị CLD có thể được đưa vào các nghiên cứu này. Favipiravir là một chất ức chế phổ rộng đường uống của RNA polymerase phụ thuộc vào RNA của virus được phê duyệt để điều trị bệnh cúm ở Nhật Bản và cho thấy một tác dụng khiêm tốn đối với COVID-19. (58) Favipiravir dường như được dung nạp tốt. (58) Tuy nhiên, một trường hợp tổn thương gan do ứ mật gây ra bởi favipiravir đã được mô tả ở một cá nhân bị tổn thương gan trước đó do ALD. Báo cáo trường hợp favipiravir này cho thấy sự liên quan của CLD cơ sở đối với các liệu pháp kháng vi-rút trong tương lai.
Tiến triển gan nhiễm mỡ và COVID-19
Tỷ lệ phổ biến NAFLD và NASH trên toàn thế giới cao, ảnh hưởng đến khoảng 25% dân số toàn cầu, khiến NAFLD / NASH trùng lặp với COVID-19 là điều không thể tránh khỏi. NAFLD có liên quan đến béo phì và các rối loạn chuyển hóa liên quan đến lối sống khác (ví dụ, bệnh tiểu đường loại 2). Kể từ khi bắt đầu đại dịch COVID- 19, béo phì và tiểu đường có liên quan đến tiên lượng bệnh xấu. (17,59) Mức độ tăng của men gan AST / ALT (≥2 × giới hạn trên của bình thường [tức là 80 U / L]) là phổ biến và có liên quan độc lập với kết quả lâm sàng bất lợi ở những bệnh nhân bị COVID-19. (60-62) Trong một nghiên cứu, tăng AST / ALT được quan sát thấy ở 235 bệnh nhân được phân loại là có COVID-19 nặng. (56 ) Một nghiên cứu khác bao gồm
31.461 người lớn mắc COVID-19, và phát hiện ra rằng bệnh gan vừa / nặng có liên quan đáng kể đến tử vong (tỷ lệ chênh lệch [OR], 2,62; khoảng tin cậy 95% [CI], 1,53 đến 4,47). (63) Trong một cuộc điều tra tương tự trên 2.780 bệnh nhân mắc COVID-19, bệnh gan lại có liên quan đáng kể đến tỷ lệ tử vong (OR, 2,8 ; KTC 95%, 1,9 đến 4,0). (64) So với bệnh nhân không có NAFLD, bệnh nhân NAFLD được báo cáo có nguy cơ tiến triển bệnh cao hơn (6,6% so với 44,7%), khả năng chức năng gan bất thường cao hơn từ khi nhập viện đến khi xuất viện (70% so với 11,1%) và lâu hơn thời gian phát tán của virus (17,5 ± 5,2 ngày so với 12,1 ± 4,4 ngày). (65) Như vậy, tỷ lệ nhiễm NAFLD cao trên toàn cầu cho thấy một phần lớn dân số có nguy cơ mắc COVID-19 nặng.
Bởi vì tiên lượng của NAFLD được xác định dựa trên mức độ nghiêm trọng của xơ hóa gan, người ta đã xem xét rằng bệnh nhân NAFLD có điểm xơ hóa gan không xâm lấn cao hơn có thể có nguy cơ mắc COVID-19 nặng hơn. Thật vậy, nguy cơ mắc COVID-19 nghiêm trọng cao hơn đáng kể ở những bệnh nhân NAFLD đã được chẩn
đoán nhiễm mỡ gan dựa trên chụp cắt lớp vi tính (OR, 4,32; KTC 95%, 1,94 đến 9,59) hoặc bị xơ hóa trung gian hoặc cao-4 ( Chỉ số FIB- 4) (OR, 5,73; KTC 95%, 1,84 đến 17,9), bất kể bệnh kèm theo chuyển hóa. (66,67) So với bệnh nhân NAFLD có điểm
FIB-4 thấp hoặc cá nhân không có NAFLD, bệnh nhân NAFLD có trung gian hoặc điểm FIB-4 cao có nhiều khả năng là người già và béo phì; mắc bệnh tiểu đường, men gan cao hơn và CRP cao hơn; và thể hiện mức độ thấp hơn của tế bào lympho, tiểu cầu, chất béo trung tính, và cholesterol lipoprotein mật độ cao. (7,8) Hơn nữa, ở những bệnh nhân có COVID-19, nhu cầu thở máy có liên quan độc lập với béo phì (OR 4,5), đái tháo đường (OR 2,55) và FIB-4 ≥ 2,67 (OR 3,09), và FIB-4 ≥ 2,67 cũng liên quan đến tăng tỷ lệ tử vong trong 30 ngày (OR, 8,4; KTC 95%, 2,23 đến 31,7). (68)
Mối liên quan giữa NAFLD / NASH và một đợt COVID-19 nghiêm trọng cho thấy khả năng điểm số nguy cơ di truyền cho NAFLD, dựa trên tác động có trọng số của các biến thể nguy cơ trong PNPLA3 (miền phospholipase giống patatin – 3) – TM6SF2 ( transmembrane 6 superfamily member 2) –MBOAT7 (protein chứa miền O-acyltransferase 7 liên kết màng) –GCKR (chất điều hòa glucokinase) trên chất béo gan trong dân số nói chung, (69) có thể ảnh hưởng đến nguy cơ COVID-19. (70) Trong một phân tích 1.460 cá nhân, trong đó 526 người dương tính và 934 người âm tính với SARS-CoV-2, điểm số nguy cơ di truyền cho NAFLD không liên quan đến việc tăng nguy cơ mắc COVID-19. Tuy nhiên, cuộc điều tra này cho thấy xu hướng bảo vệ chống lại COVID-19 được tạo ra bởi đa hình nucleotide rs738409, mã hóa biến thể p.I148M PNPLA3, biểu hiện gan cao hơn của các thụ thể SARS-CoV-2 ACE2 và TMPRSS2, (71,72), điều này có thể giải thích diễn biến lâm sàng tồi tệ hơn của những bệnh nhân này. Một nghiên cứu cho thấy NAFLD / NASH không ảnh hưởng đến biểu hiện gan của gen ACE2 và TMPRSS2. COVID-19. (73) Hệ vi sinh vật đường ruột và các sản phẩm oxy hóa axit béo không hoàn toàn cũng liên quan đến NAFLD / NASH và COVID-19 nghiêm trọng, (74-76) có thể bằng cách điều chỉnh phản ứng miễn dịch của vật chủ. (77)
Trong bối cảnh của COVID-19, nó đã được chứng minh rõ ràng rằng sự hiện diện của NAFLD /NASH khiến bệnh nhân có tỷ lệ mắc và tử vong do COVID-19 nghiêm trọng. Bởi vì không có các liệu pháp đã được phê duyệt cho NAFLD / NASH, nhiều thử nghiệm đang được tiến hành trong lĩnh vực nghiên cứu lâm sàng này. Tuy nhiên, nhiều cuộc thử nghiệm như vậy đã bị gián đoạn do đại dịch COVID-19. Mức độ phổ biến cao trên toàn cầu của CLD đảm bảo sự tiếp tục của các thử nghiệm NAFLD / NASH đang diễn ra.(78)
Bệnh gan liên quan đến rượu
ALD có liên quan độc lập với nguy cơ tử vong tăng 1,8 lần ở bệnh nhân COVID-19.
(11) Hơn nữa, bệnh nhân mắc cả ALD và COVID-19 dường như có biểu hiện tổn thương gan nặng hơn, vì tỷ lệ bệnh nhân không bị xơ gan chỉ là 6% ở bệnh nhân ALD so với 62% ở những người bị NAFLD. ( 11) Một báo cáo trường hợp mô tả 2 bệnh nhân được chẩn đoán nhiễm trùng COVID-19 tại bệnh viện và viêm phổi COVID-19 nặng khi nhập viện trong thời gian điều trị ALD. (79) Cả hai bệnh nhân đều phát triển suy đa phủ tạng và tử vong trong một thời gian ngắn. Một nghiên cứu bổ sung chỉ ra rằng nguy cơ mắc COVID-19 nghiêm trọng có liên quan đáng kể đến tổn thương gan do rượu (OR, 7,05; KTC 95%, 6,30-7,88) và xơ gan do rượu (OR, 7,00; KTC 95%, 6,15 đến 7,97). (80) Tuy nhiên, rất ít nghiên cứu đã khám phá tác động của rượu trong đại dịch COVID-19, cũng như các cơ chế mà qua đó uống rượu và ALD có thể ảnh hưởng đến cơ chế bệnh sinh COVID-19. (81)
Uống quá nhiều rượu có thể có tác dụng điều hòa miễn dịch và khiến người bệnh dễ mắc các bệnh nhiễm trùng do vi rút và vi khuẩn. (82,83) Người ta ước tính rằng rượu gây ra 3,3 triệu ca tử vong hàng năm. (84) Nhiều bệnh lý có liên quan đến uống rượu, với CLD và xơ gan là những vấn đề sức khỏe chính liên quan đến rượu. Thật không may, mức tiêu thụ rượu đang cho thấy sự gia tăng hàng năm gần như trên toàn thế giới. (84) Hơn nữa, các biện pháp ngăn cách và ngăn cản xã hội dẫn đến việc lạm dụng rượu gia tăng, làm trầm trọng thêm bệnh CLD liên quan đến rượu và tổn thương gan. (85)
Theo Miguel Angel Martinez , and Sandra Franco
PGS. TS. BS. Phạm Thị Thu Thủy
Trưởng khoa Gan, Trung tâm Chẩn đoán y khoa Medic TP. HCM
REFERENCES
1) Fajgenbaum DC, June CH. Cytokine storm. N Engl J Med 2020;383:2255-2273.
2) Sinha P, Matthay MA, Calfee CS. Is a “cytokine storm” relevant to COVID-19? JAMA Intern Med 2020;180:1152-1154.
3) Dexamethasone in hospitalized patients with Covid-19— preliminary report. N Engl J Med2021;384:693-704.
4) Moore JB, June CH. Cytokine release syndrome in severe COVID-19. Science 2020;368:473-474.
5) Huang C, Wang Y, Li X, Ren L, Zhao J, Hu YI, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan. China Lancet 2020;395:497-506.
6) Del Valle DM, Kim-Schulze S, Huang HH, Beckmann ND, Nirenberg S, Wang B, et al. An inflammatory cytokine signature predicts COVID-19 severity and survival. Nat Med 2020;26:1636-1643.
7) Sepanlou SG, Safiri S, Bisignano C, Ikuta KS, Merat S, Saberifiroozi M, et al. The global, regional, and national burden of cirrhosis by cause in 195 countries and territories, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet Gastroenterol Hepatol 2020;5:245-266.
8) Asrani SK, Devarbhavi H, Eaton J, Kamath PS. Burden of liver diseases in the world. J Hepatol 2019;70:151-171.
9) Racanelli V, Rehermann B. The liver as an immunological organ. Hepatology 2006;43:S54-S62.
10) Albillos A, Lario M, Álvarez-Mon M. Cirrhosis-associated immune dysfunction: distinctive features and clinical relevance. J Hepatol 2014;61:1385-1396.
11) Marjot T, Moon AM, Cook JA, Abd-Elsalam S, Aloman C, Armstrong MJ, et al. Outcomes following SARS-CoV-2 infection in patients with chronic liver disease: an international registry study. J Hepatol 2020;74:567-577.
12) Webb GJ, Marjot T, Cook JA, Aloman C, Armstrong MJ, Brenner EJ, et al. Outcomes following SARS-CoV-2 infection in liver transplant recipients: an international registry study. Lancet Gastroenterol Hepatol 2020;5:1008-1016.
13) Bertolini A, van de Peppel IP, Bodewes FAJA, Moshage H, Fantin A, Farinati F, et al. Abnormal liver function tests in patients with COVID-19: relevance and potential pathogenesis. Hepatology 2020;72:1864-1872.
14) Templin C, Ghadri JR, Diekmann J, Napp LC, Bataiosu DR,Jaguszewski M, et al. Clinical features and outcomes of Takotsubo (Stress) cardiomyopathy. N Engl J Med 2015;373:929-938.
15) Phipps MM, Barraza LH, LaSota ED, Sobieszczyk ME, Pereira MR, Zheng EX, et al. Acute liver injury in COVID-19: prevalence and association with clinical outcomes in a large U.S. cohort. Hepatology 2020;72:807-817.
16) Goyal P, Choi JJ, Pinheiro LC, Schenck EJ, Chen R, Jabri A, et al. Clinical characteristics of Covid-19 in New York City. N Engl J Med 2020;382:2372-2374.
17) Richardson S, Hirsch JS, Narasimhan M, Crawford JM, McGinn T, Davidson KW, et al. Presenting characteristics, comorbidities, and outcomes among 5700 patients hospitalized with COVID-19 in the New York City area. JAMA 2020;323:2052-2059.
18) Hoffmann M, Kleine-Weber H, Schroeder S, Krüger N, Herrler T, Erichsen S, et al. SARSCoV-2 cell entry depends on ACE2 and TMPRSS2 and is blocked by a clinically proven protease inhibitor. Cell 2020;181:e8.
19) De Smet V, Verhulst S, van Grunsven LA. Single cell RNA sequencing analysis did not predict hepatocyte infection by SARSCoV-2. J Hepatol 2020;73:993-995.
20) Zou X, Chen K, Zou J, Han P, Hao J, Han Z. Single-cell RNAseq data analysis on the receptor ACE2 expression reveals the potential risk of different human organs vulnerable to 2019- nCoV infection. Front Med 2020;14:185-192.
21) Qi F, Qian S, Zhang S, Zhang Z. Single cell RNA sequencing of 13 human tissues identify cell types and receptors of human coronaviruses. Biochem Biophys Res Commun2020;526:135-140.
22) Chai X, Hu L, Zhang Y, Han W, Lu Z, Ke A, et al. Specific ACE2 expression in cholangiocytes may cause liver damage after 2019-nCoV infection. bioRxiv 20;2020.02.03.931766.
23) Hamming I, Timens W, Bulthuis MLC, Lely AT, Navis GJ, van Goor H. Tissue distribution of ACE2 protein, the functional receptor for SARS coronavirus. A first step in understanding SARS pathogenesis. J Pathol 2004;203:631-637.
24) Hikmet F, Méar L, Edvinsson Å, Micke P, Uhlén M, Lindskog C. The protein expression profile of ACE2 in human tissues. Mol Syst Biol 2020;16:e9610.
25) Pirola CJ, Sookoian S. SARS-CoV-2 virus and liver expression of host receptors: putative mechanisms of liver involvement in COVID-19. Liver Int 2020;40:2038-2040.
26) Chu H, Chan J-W, Yuen T-T, Shuai H, Yuan S, Wang Y, et al. Comparative tropism, replication kinetics, and cell damage profiling of SARS-CoV-2 and SARS-CoV with implications for clinical manifestations, transmissibility, and laboratory studies of COVID-19: an observational study. Lancet Microbe 2020;1:e14-e23.
27) Wang Y, Liu S, Liu H, Li W, Lin F, Jiang L, et al. SARS-CoV-2 infection of the liver directly contributes to hepatic impairment in patients with COVID-19. J Hepatol 2020;73:807-816.
28) Philips CA, Ahamed R, Augustine P. SARS-CoV-2 related liver impairment—perception may not be the reality. J Hepatol 2020;73:991-992.
29) Redd WD, Zhou JC, Hathorn KE, McCarty TR, Bazarbashi AN, Thompson CC, et al. Prevalence and characteristics of gastrointestinal symptoms in patients with severe acute respiratory syndrome coronavirus 2 infection in the United States: a multicenter cohort study. Gastroenterology 2020;159:765-767.e2.
30) Lamers MM, Beumer J, Van Der VJ, Knoops K, Puschhof J, Breugem TI, et al. SARS-CoV2 productively infects human gut enterocytes. Science 2020;369:50-54.
31) Wang W, Xu Y, Gao R, Lu R, Han K, Wu G, et al. Detection of SARS-CoV-2 in different types of clinical specimens. JAMA 2020;323:1843-1844
32. Zhang W, Du R‐H, Li B, Zheng X‐S, Yang X‐L, Hu B, et al. Molecular and serological investigation of 2019‐nCoV





